경제
폐암 치료제 ‘렉라자’, K-항암제 최초 FDA 승인
- 0
- 가
- 가
리브리반트와 병용으로 허가 승인
유럽·중국·국내 처방에도 긍정적
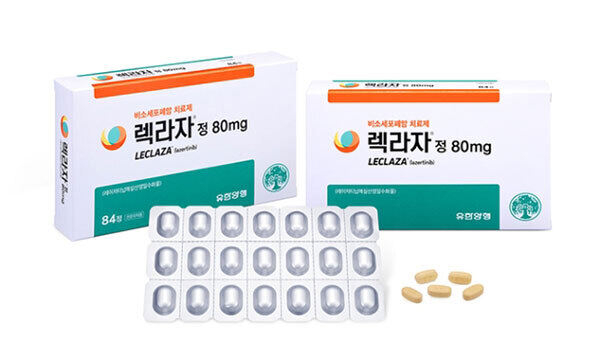
[마이데일리 = 박성규 기자] 국산 신약 31호인 유한양행의 폐암 치료제 ‘렉라자(레이저티닙)’가 미국 식품의약국(FDA)의 승인을 받아냈다.
21일 유한양행은 미국 FDA가 렉라자와 존슨앤드존슨(J&J)의 리브리반트(성분명 아미반타맙) 정맥주사(IV) 병용요법을 국소 진행성·전이성 비소세포폐암(NSCLC) 환자 대상 1차 치료제로 승인했다고 밝혔다.
이 3상 연구에서, 리브리반트와 렉라자 병용요법은 오시머티닙 단독요법에 비해 질병 진행 또는 사망위험을 30% 감소시켰다. 또한 무진행 생존기간(PFS)은 23.7개월로, 오시머티닙의 16.6개월 보다 길었다.
이번 승인으로 렉라자와 리브리반트의 병용요법은 상피세포성장인자수용체(EGFR) 변이 NSCLC 환자의 1차 치료제로 승인된 오시머티닙 대비 우월성을 입증한 최초이자 유일한 다중 표적, 비화학요법 병용요법이 됐다.
이번 FDA승인으로 유한양행은 R&D에서 오픈이노베이션의 첫 결실을 맺게 됐다. 2021년 1월 국산신약 제31호 신약으로 허가 받은 비소세포폐암 치료제인 렉라자는 23년 6월 국내 1차 치료제로 허가가 확대된 이후 6개월 만에 건강보험 급여 적용을 받아 24년 1분기 처방 약 200억원을 달성했다.
이번 FDA에서 리브리반트의 병용요법 허가로 인해 승인심사를 앞두고 있는 유럽, 중국, 일본은 물론 국내에서도 렉라자의 처방에 긍정적인 영향을 줄 것으로 기대된다.
조욱제 유한양행 사장은 “이번 승인이 종착점이 아닌 하나의 통과점이 되어 R&D투자를 통해 한국을 대표하는 글로벌 혁신신약 출시와 함께 유한양행의 글로벌 탑 50 달성을 위한 초석이 됐으면 한다”고 말했다.
박성규 기자 psk@mydaily.co.kr
- ⓒ마이데일리(www.mydaily.co.kr).
무단전재&재배포 금지 -


















댓글
[ 300자 이내 / 현재: 0자 ]
현재 총 0개의 댓글이 있습니다.